Kan den lille sebrafisken være nøkkelen til behandling av hjernekreft?
NTNU, Trondheim
Hjernen er et fascinerende organ som styrer alt vi gjør, våre tanker, følelser og adferd. Slik som andre organer i kroppen kan også hjernen rammes av sykdom.

Illustrasjonsfoto: Getty Images
Når det oppstår endringer i hjernen, kan dette få omfattende konsekvenser for oss og resulterer ofte i fysiske og kognitive funksjonsnedsettelser som videre kan føre til redusert livskvalitet. Dette bidrar til at hjernesykdommer ofte oppleves som svært skremmende og dypt urovekkende for mange. Vi er forskere ved NTNU i Trondheim med lang erfaring innen hjerneforskning. På laboratoriet vårt er vi svært interessert i å undersøke de prosessene som påvirker hjernens utvikling og funksjonen under fosterstadiet og ved sykdom. Mye av vår forskning fokuserer nettopp på den syke hjernen. Ett av de sentrale prosjektene gruppen vår jobber med, er analyse av pasient-spesifikke egenskaper som videre kan bidra til utvikling av mer pasient tilpasset behandling av glioblastom. For å oppnå formålet med vår forskning bruker vi en fisk, sebrafisken, som modellorganisme.
Støtteceller til nytte og besvær
For å bedre forstå hjernen, er det viktig å ha kunnskap om cellene den er bygd opp av. Når man hører om hjernen, er det som regel nevronene, også kjent som nerveceller, som trekkes frem. Dette er de mest kjente cellene i hjernen, og de spiller uten tvil en helt sentral rolle for hjernens funksjon. Gjennom et enormt nettverk av forbindelser gjør nevronene oss i stand til å sanse verden rundt oss, bearbeide informasjon og bevege kroppen. Nevronene er ikke de eneste cellene som befinner seg i hjernen; de er nemlig omgitt av mange andre celletyper med ulike essensielle funksjoner og oppgaver. Sammen sørger disse cellene for at hjernen fungerer slik den skal. En av disse celletypene er gliacellene, som fungerer som støtteceller for nevroner. Noen av de mest sentrale funksjonene til glia er å gi næring til nevroner og kontrollere kontaktpunktene mellom disse cellene. I tillegg bidrar de til produksjon av myelin som fungerer som isolasjon rundt aksonene. Glia er dermed essensielle for den normale funksjonen til hjernen.
Gliaceller har ikke bare en støtterolle i hjernen, noen av de kan faktisk fungere som stamceller og gi opphav til nye nevroner. Stamceller og glia gjennomgår veldig få celledelinger etter fødsel og forekomsten reduseres ytterligere med alderen. Selv om celledelingen forekommer på en svært kontrollert måte, kan det forekomme feil. Mutasjoner kan oppstå og føre til at gliacellene begynner å dele seg på en ukontrollert måte. Dette kan videre føre til utvikling av hjernesvulst og i verste fall kreft slik som for eksempel gliom. Den mest aggressive formen for gliom er glioblastom. Det er nettopp denne krefttypen vi retter forskningen vår mot på laboratoriet i Trondheim. Glioblastom kjennetegnes av rask vekst og høy infiltrering av hjernen. Pasienter diagnostisert med glioblastom har en kort forventet levetid, hvor sannsynligheten for å overleve mer enn 15 måneder er veldig lav. En slik diagnose har en svært dårlig prognose. Uten en kur tilgjengelig, er glioblastomdiagnosen en dødsdom. Når diagnosen stilles, rammer det ikke bare pasienten, men også familien og de nærmeste rundt. Årlig diagnostiseres over 200 nordmenn av glioblastom. Blant disse er det menn som rammes hyppigst. Median alder ved diagnose er 65 år, men i prinsippet kan alle rammes. Disse prognosene og tallene ønsker vi å gjøre noe med.
Behandlingsresistente celler
Kreftbehandling hargjort store fremskritt i løpet av desiste årene. Med disse fremskrittene kan flere kreftpasienter leve flere tiår etter å ha fått en kreftdiagnose. De får leve et godt og langt liv, bli eldre og møte barnebarn. Fremskrittene gir håp for kreftpasienter og en ny sjanse til å leve et fullverdig liv. Denne progresjonen i kreftbehandling gjelder for mange ulike kreft typer, men dessverre ikke glioblastom hvor situasjonen er helt annerledes. Hvor ligger forskjellen? Hvorfor kan noen krefttyper behandles og holdes i sjakk, mens andre resulterer i død? Behandlingen av glioblastom består vanligvis av kirurgisk reseksjon av svulsten etterfulgt av cellegift (temozolomide) og strålebehandling. Til tross for denne aggressive og intensive behandlingsmetoden blir pasienter sjelden kurert, og tilbakefall er uunngåelig. Noen av cellene klarer å overleve behandlingen og får dermed anledning til å endre, tilpasse og spre seg videre i hjernen. Som en konsekvens utvikler cellene resistens mot behandling,noe som gjør det vanskelig å stoppe sykdommen og reduserer sjansen for overlevelse, betydelig.
Mange forskere rundt om i verden har prøvd å kartlegge glioblastom ytterligere, og bruke denne informasjonen til å utvikle nye, mer pasientspesifikke behandlingsalternativer. Likevel er overlevelsesraten blant glioblastom pasienter fortsatt lav. Et stort problem som hindrer fremgang i behandling av pasienter, er metodene som brukes for å studere glioblastom på laboratoriet. Pasientceller isoleres fra biopsier etter kirurgisk reseksjon og dyrkes videre i petriskåler ved bruk av standard celledyrkningsmetoder. Disse metodene har blitt brukt i en årrekke og har ført til oppdagelse av mange nye og lovende legemidler. Likevel ser man ikke denne lovende effekten når medisinene testes på pasienter i klinikken. Sjeldent gir disse gode resultater. Hvorfor skjer dette?
Kompliserte variasjoner og samspill
En del av problemet ligger i det at kreftcellene som isoleres fra pasienter har høy molekylær og cellulær heterogenitet. Når disse dyrkes i petriskåler opprettholdes ikke denne heterogeniteten og cellene mister sin normale funksjon. I petriskålen mister cellene kontakten med andre viktige celler og komponenter som vanligvis er til stede i hjerne, dette inkluderer nevroner og immunceller, men også blodårer. Mange av komponentene i tumormikromiljøet kan heller ikke replikeres in vitro. Uten disse interaksjonene reduseres den cellulære heterogeniteten som videre fører til at cellene ikke lenger er representative for den opprinnelige tumoren. Flere studier viser viktigheten av å bevare tumormikromiljøet for å bedre forstå glioblastom. Gjennom årene har forsk-ere utviklet forskjellige modeller som nettopp replikerer dette unike miljøet i både dyr og tumoroider. Disse modellene er generert direkte fra kirurgiske biopsier og gir dermed et mer realistisk bilde på hvordan kreften oppfører seg og den høye heterogeniteten. Dette legger til rette for grundig kartlegging av pasientspesifikke karakteristikker og dermed åpner for pasientspesifikk behandling av glioblastom.
Fra akvariet til laboratoriet
På laboratoriet vårt i Trondheim jobber vi med en liten fisk bedre kjent som sebrafisken. Arten kommer opprinnelig fra India, men har i flere tiår vært en populær akvariefisk. Siden 1990-tallet har sebrafisken også etablert seg som en av de mest brukte dyremodellene innen biologisk og medisinsk forskning, med over tusen laboratorier verden rundt som benytter den. Hvorfor er denne lille fisken så ettertraktet? Og hva gjør den så populær? Svaret er veldig enkelt – den er gjennomsiktig. Denne unike egenskapen gir forskere innsikt i hva som foregår i kroppen, helt ned på cellenivå, mens fisken lever og beveger seg under mikroskopet. Dette gjør det mulig for forskere som oss å måle aktiviteten til hver eneste celle i sebrafiskens hjerne mens den svømmer, blir eksponert for lukt, lys og vibrasjon, med mer.
Sebrafisken er et virveldyr, akkurat som oss mennesker. I tillegg deler den mye av den genetiske informasjonen og mange av de samme utviklingsprosessene. Dette gjør den til en verdifull og enestående modell for forskning på menneskelige sykdommer. Forskning på sebrafisken har bidratt til en bedre forståelse av hvordan sykdom oppstår, og har også spilt en viktig rolle i utviklingen av flere medisiner som i dag brukes i behandling av ulike sykdommer. Derfor blir det naturlige spørsmålet: kan vi også studere glioblastom ved hjelp av sebrafisken? Stadig flere studier tyder på at svaret er ja.
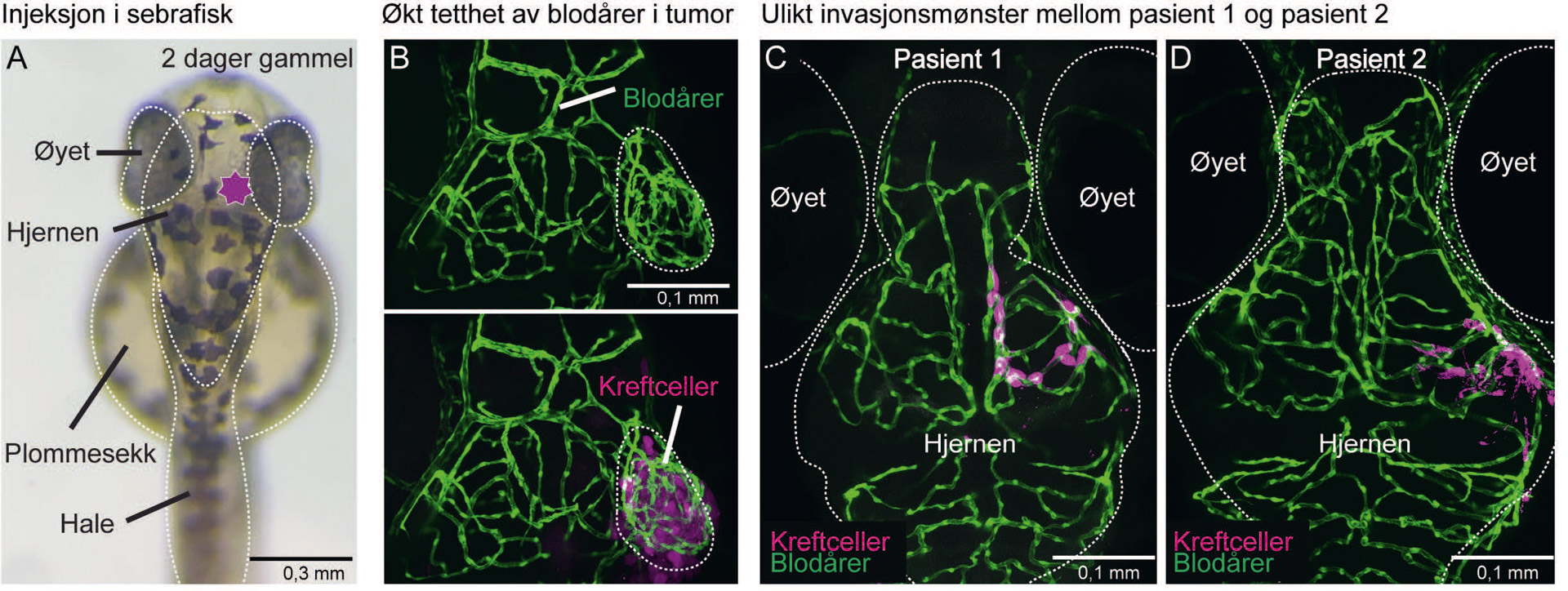
(A) Bilde av en to dager gammel sebrafisk gjennom et mikroskop. Stjernen ndikerer hvor i hjernen pasientceller blir injisert. (B) Etter en tre dagers inkubasjonstid har kreftcellene klart å rekruttere sebrafiskens blodårer til tumoren. Dette indikererer at cellene trives i sebrafisken og er i stand til å få næring og dermed fortsette å vokse. Resultater fra invasjonsforsøk viser tydelige forskjeller i invasjonsmønsteret til celler fra pasient 1 (C) og pasient 2 (D). Resultatene viser også hvor ulike cellene er.
Hjerner har mye til felles
Selv om sebrafisken ikke er et pattedyr, kan man introdusere menneskelige kreftceller i sebrafiskens hjerne og se hvordan cellene oppfører seg i en levende organisme. Våre resultater, i tråd med funn fra andre forskningsgrupper, viser at tumorcellene trives i sebrafiskhjernen. De er i stand til å rekruttere blodårer til tumoren for å sikre seg næring, på samme måte som i menneskehjernen. Vi startet med disse eksperimentene for to år siden og kan allerede se at celler fra ulike pasienter oppfører seg annerledes. Noen er svært aggressive og invaderer andre hjerneregioner mens andre forblir der de ble transplantert. I dag samarbeider vi med forskningsgrupper i både Norge og utlandet for å undersøke om vi kan forutsi sykdomsutvikling basert på hvordan kreftcellene oppfører seg i sebrafiskhjernen. Parallelt har vi begynt å teste nye medisiner som skal hindre kreftcellene i å dele og sprer seg, samtidig som vi passer på at fisken tåler behandlingen uten noen bivirkninger. Vår ambisjon er at modellen skal bidra til en raskere og mer målrettet medisinsk utvikling i fremtiden, uten at det skal gå på bekostning av sebrafiskens livskvalitet og helse.
Kan den lille sebrafisken være nøkkelen til behandling av glioblastom? Kan sebrafisken bli en del av pasienttilpasset diagnostikk? En studie fra Rita Fiors laboratorium i Portugal har allerede vist at sebrafisken kan gi leger verdifull støtte under valg av riktig kreftmedisin for pasienter, bare ti dager etter at biopsien er isolert. Vi ved NTNU, er fortsatt i startfasen av vårt glioblastom studie, og går inn i dette arbeidet med et sterkt håp om betydningsfulle resultater i fremtiden. Funnene vi allerede har gjort gir oss både motivasjon og tro på at vi er på rett vei. Vi vet at veien fra laboratoriet til behandling av pasienter er lang og krevende. Likevel håper vi at forskningen vår kan bringe oss et skritt nærmere en fremtid der flere pasienter får bedre behandlingsmuligheter og kanskje en dag, håp om et liv uten glioblastom.
Ordliste
Biopsier: vevsprøver som har blitt isolert fra en pasient og ofte brukes for videre undersøkelser, vanligvis for å stille diagnose.
Heterogenitet: beskriver ulikheten eller mangfoldet av celler i en kreftmasse. Begrepet beskriver hvor forskjellige cellene er fra hverandre i utseende, egenskaper, genetikk osv…
In vitro: betyr «i glass» og refererer til eksperimenter utført under kontrollerte forhold på et laboratorium, utenfor organismen. Dette kan for eksempel være i reagensrør eller cellekulturplater.
Modellorganisme: kan referere til organismer slik som bakterier, mus, sopp, fisk osv… som brukes på laboratoriet for å forstå sykdomsmekanismer, biologiske prosesser og mer.
Myelin: er et isolerende fettrikt lag som omslutter nervefibrene og videre bidrar til å øke hastigheten på elektriske signaler i nervesystemet.
Reseksjon: kirurgisk fjerning av deler av syke organer. Formålet er å fjerne for eksempel svulster.
Stamceller: er celler som kan fornye seg selv og videre utvikles til spesialiserte celletyper.
Tumormikromiljø: er et begrep som beskriver det komplekse støttevevet som omgir en svulst. Dette miljøet består ofte av immunceller, blodkar og andre vekstfaktorer som er nødvendig for tumorens vekst, overlevelse og spredning.